2020年10月1日腸サイト投稿から移動
(1)腸内細菌叢は一つの臓器
ヒトの体細胞は約37兆個といわれていますが、ヒトの体の外にあたる腸管内には約100兆個という宿主を構成している細胞より多くの腸内細菌が生存しています※1。その腸内細菌は腸管内にただ生存しているのではなく、腸内細菌叢に異常が生じると、ヒトでもイヌネコでも病気になることが多く、現在では腸内細菌叢は独特の代謝能力を備えた臓器として認識されています。一例として、腸内細菌叢が腸管粘膜の免疫に与える作用について図を下に、図の説明を補足説明に載せました※2, ※3。
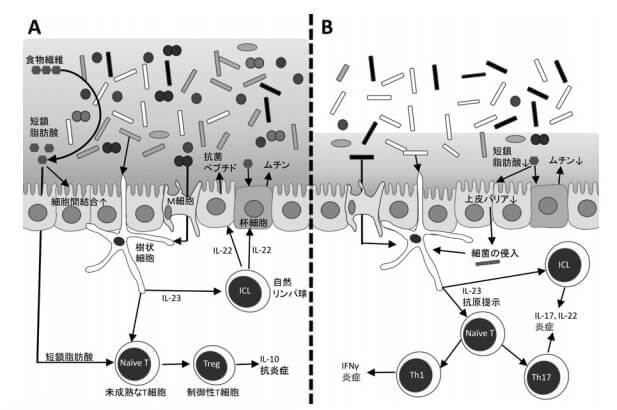
左が恒常性を保っている状態(symbiosis)で、右が腸内細菌叢のバランスが崩れ、慢性炎症が発生している状態(dysbiosis)です。
(2)腸内細菌叢の異常とは
①腸内細菌叢の異常とは
腸内細菌叢の異常には2種類あります。腸内細菌の数の異常(増えすぎ、減りすぎ)と質の異常(菌叢の構成バランスの異常)です※2。
「数の異常」にはヒトとペットでSIBO(小腸内細菌過剰増殖)が知られています。また、腐敗した食べ物を食べ、食中毒菌などが一時的に増殖することも「数の異常」に含まれますが、免疫機能が正常に機能していれば、下痢等で原因菌を体外に排泄し、その後菌数は正常に戻ります。
「質の異常(菌叢の構成バランスの異常、ディスバイオシス)」に関しては、近年のDNA解析技術の向上により病気と腸内細菌叢の変化や代謝物質の変化などの研究が進んでおり※4、腸内細菌叢の異常が原因だと考えられていなかった生活習慣病(肥満、糖尿病、動脈硬化など)や神経系の病気まで、現在では腸内細菌叢の構成バランスの異常が原因と考えられてきています。
②腸内細菌叢の質の異常による慢性炎症
ではなぜ腸内細菌叢の質の異常(ディスバイオシス)から様々な病気が引き起こされるのでしょうか?それはディスバイオシスは長期にわたることが多く、長期にわたって上の図に示したような免疫機能に悪影響を与え、慢性炎症になりやすいためです。一時的なディスバイオシスは「数の異常」にもあたりますが、免疫機能が正常であれば、数日間で元の状態に戻り、問題は起こりません。しかしディスバイオシスが長期に継続する場合は、バランスの崩れた腸内細菌による代謝産物の不足や過剰(表※5)により、その代謝産物や腸内細菌そのものが体内に侵入し、免疫機能のバランスも乱し、慢性的な炎症を引き起こします。腸内細菌が生成する代謝産物とその働きの一覧を表に載せました。
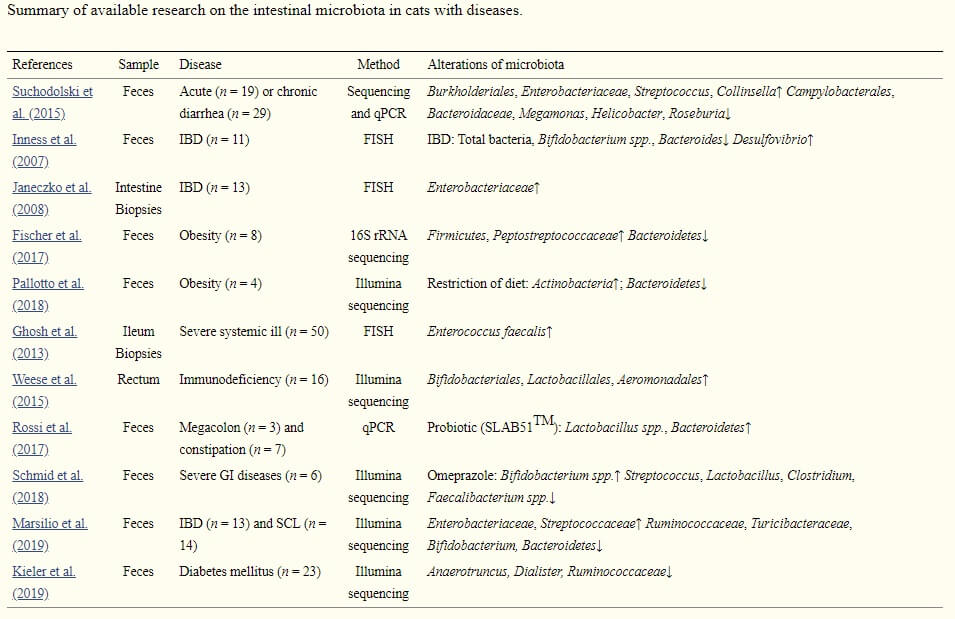
(画像が悪いので、元文献のリンクはこちらです。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7329990/table/T1/?report=objectonly )
生成物は上から、短鎖脂肪酸(酢酸)、プロピオン酸、酪酸、インドール、ポリアミン、イソ酪酸、硫化水素、尿毒症毒素(インドキシル硫酸など)、オクタデセン酸です。この表に載っていませんが、油を分解するときに必要な胆汁に含まれている胆汁酸を変換した二次胆汁酸(大腸がんのプロモーター)も腸内細菌の生成物です。このように宿主によい働きをする物質と悪影響を与える物質があります。
この中の短鎖脂肪酸の生成量が減少すると、腸上皮の栄養源が不足し、腸上皮細胞同士を結合しているタイトジャンクションが緩み、腸内細菌が生成した毒素物質と、腸内細菌そのものが体内に入り、慢性炎症になります。わかりやすい図を下に貼りました※5。
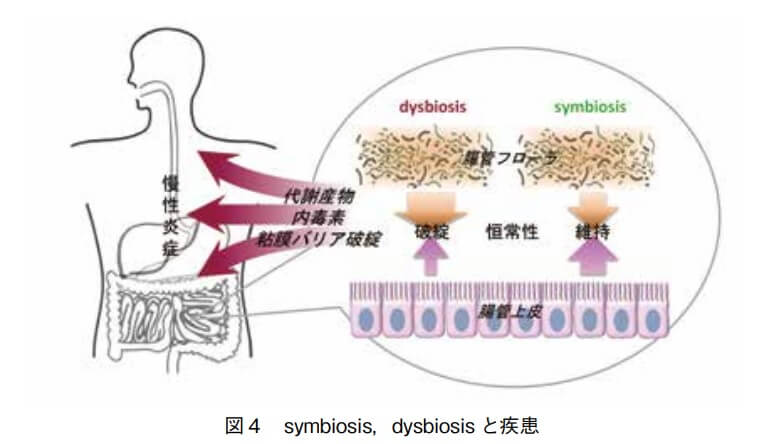
右側が、腸内細菌叢のバランスがとれている(symbiosis)状態です。一方、左側は、腸内細菌叢のバランスが異常な状態(dysbiosis, ディスバイオシス)で、この状態が続くと、粘膜バリアが破綻して、腸内細菌が生成した代謝産物や内毒素等が体内に入り、宿主の全身性の慢性炎症やそれに続く各種疾患の発症の原因となると考えられています。
ヒトでは、近年の研究から、以下の図のように腸疾患だけではなく、免疫関連疾患(アレルギー、自己免疫疾患)、代謝内分泌疾患(肥満、糖尿病、脂肪肝、動脈硬化)、神経関連疾患(多発性硬化症、自閉症、うつ、パーキンソン病、ALS)など様々な疾患と腸内細菌叢との関連が報告されています※6。
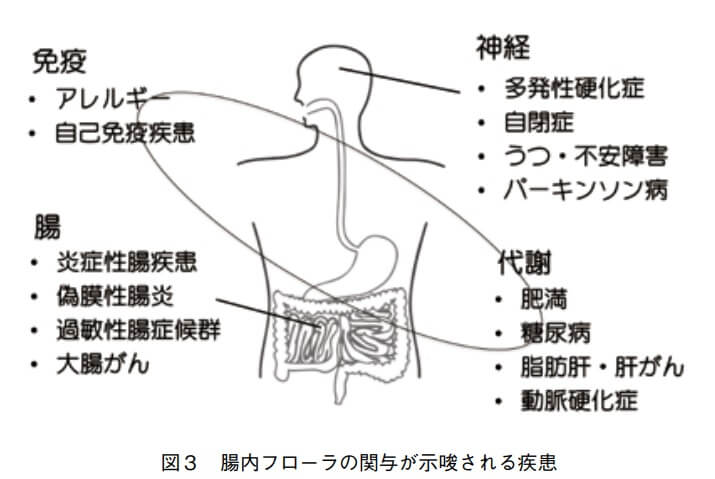
(3)イヌネコもヒトと同じか?
ヒトとイヌやネコの腸内細菌叢は似ています。ヒトとイヌネコの腸内細菌の共通な主な門は、ファーミキューテス、バクテロイデス、プロテオバクテリア、アクチノバクテリアで、イヌネコなど肉食動物にはフソバクテリア門に属する細菌が多く占めています。
詳しくはこちらをご覧ください https://arterio.co.jp/2023/03/10/cat-intestinal-microbiota/
ヒトと同じく、イヌネコでも、腸内細菌が腸まで届く難消化性物質を利用して生成する代謝産物には、ビタミン、短鎖脂肪酸、二次胆汁酸、その他の細菌由来化合物があり、これら代謝産物が免疫細胞と炎症機能に影響を与え、消化器系だけではなく、全身の神経系、腎臓系、皮膚系、内分泌系、免疫系、呼吸器系を含む主要な宿主系の調節に影響を与えます。そのため、全身の慢性炎症が全身の病気の原因になることが示唆されています※5。
ディスバイオシスが関係する病気の研究には、炎症性腸疾患、アレルギー、便秘、歯周病、肥満、糖尿病、腎臓病などがあります。この中で、糖尿病は、ネコイヌの有病率が増加しており、ディスバイオシスがネコイヌの2型糖尿病の発症に関連していることもわかってきました。たとえば、糖尿病のネコは同じ年齢の健康なネコと比較して、腸内細菌の多様性が大幅に減少し(ディスバイオシスでは多様性が減少する)、酪酸菌が失われることも示されています。また、慢性腎臓病(CKD)もネコイヌで最も一般的な病気の1つですが、慢性腎臓病に関しても、慢性腎臓病のネコは健康なネコと比較して腸内細菌の数と多様性が減少していることが示されました※5。
ネコの病気と腸内細菌叢の研究の一覧を以下に貼りました※8。
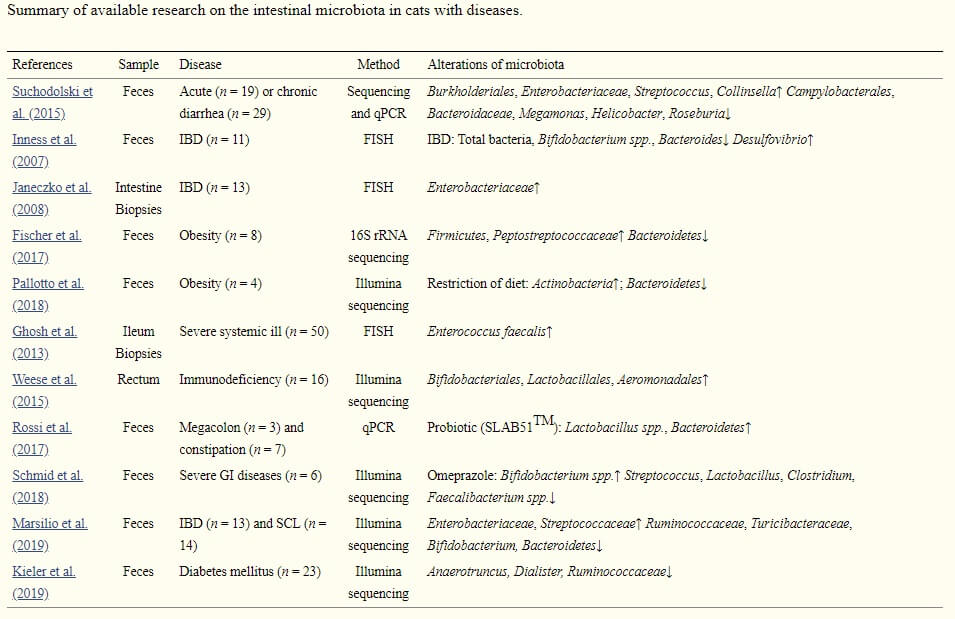
上から、病名は、急性慢性下痢、IBD,IBD、肥満、肥満、重度の全身性疾患、免疫不全、巨大結腸症と便秘、重度の腸疾患、IBDとSCL、糖尿病です。
こちらも画像は悪いので、こちらをご覧ください。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7393142/table/T3/?report=objectonly
短鎖脂肪酸(酪酸)が免疫のバランスを整えることは以前の一般人向けの記事で書きましたので、こちらをご覧ください。https://arterio.co.jp/2018/01/29/butyric-acid/
https://arterio.co.jp/2019/06/12/dysbiosis/
免疫の超簡単な説明はこちらです
https://arterio.co.jp/2016/12/05/akudama3/
IBDなど慢性腸炎はディスバイオシスから起こる慢性炎症で、免疫を抑制する細胞(Treg)を誘導する酪酸が少ないというのがヒトでもイヌネコでも定説です。今回検索したところ、慢性腸炎のイヌでは、健康なイヌと比較して、酪酸の割合は変化せずに、酢酸の割合が増加しプロピオン酸の割合が減少していたという論文もありました。これがイヌだけなのかが気になります※7。
(4)まとめ
下痢や便秘はただ便や糞がでないだけの問題ではありません。便や糞の状態は、腸内細菌叢の構成バランスが正常かどうかの指標です構成バランスが異常な状態が長期間続く場合は、宿主の免疫機能が破綻し、慢性炎症になり、様々な病気に罹患することがわかってきましたので、まずは腸内細菌叢のバランスを正常に戻し、免疫機能を整えることが重要です。
(5)補足説明と参考文献
※1 Bianconi E et al. An estimation of the number of cells in the human body. Ann Hum Biol. 2013;40:463-471.
※2 五十嵐寛高 犬や猫における腸内細菌叢と消化器疾患. ペット栄養学会誌. 2018;21:145-151.
https://www.jstage.jst.go.jp/article/jpan/21/3/21_145/_pdf/-char/ja
※3 図の説明
左が恒常性を保っている状態(symbiosis)で、右が腸内細菌叢のバランスが崩れ、慢性炎症が発生している状態(dysbiosis)です。
左は、宿主が腸まで届く難消化性物質を必要量食することにより、多様な腸内細菌が管腔内に存在しています。それらを直接またはM細胞を介して樹状細胞が認識し、病原性か否かを識別したうえで、免疫的な排除(IL-22を介したムチン・抗菌ペプチドの産生)、または抗炎症反応(制御性T細胞(Treg)の分化・誘導)が行われています。また腸内細菌叢が産生する短鎖脂肪酸は腸上皮細胞間接着(タイトジャンクション)の亢進やムチンの産生亢進といった粘膜バリアの増強と、Treg細胞の分化の双方に寄与しています。
右は、宿主が腸まで届く難消化性物質を必要量食していないことにより、腸内細菌叢のバランスが崩れ、菌叢の多様性が失われています。この状態では樹状細胞は抗原提示を介してTh1細胞やTh17細胞への分化を促進するようになり、Il-17やIL-22、IFNγといった炎症性サイトカインが多く産生されることで腸炎が発生すると考えられています。さらに短鎖脂肪酸生成菌が減少し、短鎖脂肪酸の産生量が減少することで、Treg細胞の分化誘導が減少すると同時に粘膜バリアの形成が弱まり、病原性菌の粘膜内侵入が更新してさらに腸炎が憎悪する悪循環に陥っていきます※2(一部改変)。
※4 小腸や大腸内の内容物はサンプリングが困難なため、ほとんどの研究は、便や糞で行い、便の菌叢=大腸の腸内細菌叢ととらえて研究を進めています。
※5 Susan M et al. The Effects of Nutrition on the Gastrointestinal Microbiome of Cats and Dogs: Impact on Health and Disease. Front Microbiol. 2020;11:1266.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7329990/
※6 大野博司. 腸内フローラの健康と病気への関わり. 亜鉛栄養治療. 2018;8:50-57.
※7 Minamoto Y et al. Fecal short-chain fatty acid concentrations and dysbiosis in dogs with chronic enteropathy. J Vet Intern Med. 2019; 33:1608–1618.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6639498/
※8 Lyu Y et al. Past, Present, and Future of Gastrointestinal Microbiota Research in Cats. Front Microbiol. 2020;11:1661.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7393142/